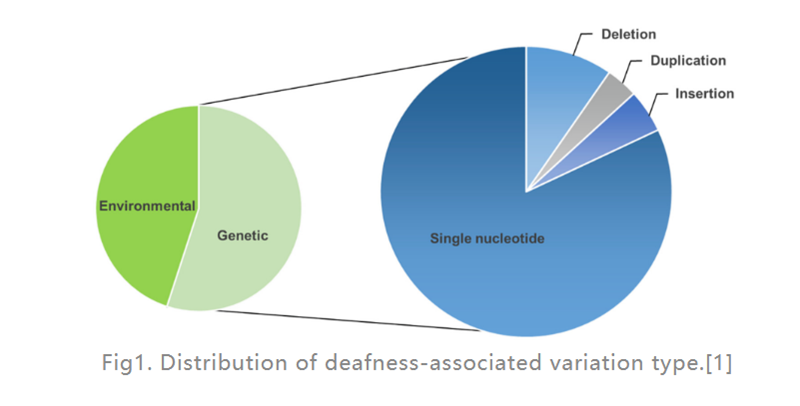
Humbja e dëgjimit (HL) është sëmundja më e zakonshme e paaftësisë shqisore tek njerëzit.Në vendet e zhvilluara, rreth 80% e rasteve të shurdhimit paragjuhësor tek fëmijët shkaktohen nga faktorë gjenetikë.Më të zakonshmet janë defektet me një gjen (siç tregohet në Fig. 1), 124 mutacione gjenesh janë gjetur të lidhura me humbjen e dëgjimit josindromik tek njerëzit, pjesa tjetër shkaktohet nga faktorë mjedisorë.Një implant koklear (një pajisje elektronike e vendosur në veshin e brendshëm që ofron stimulim elektrik drejtpërdrejt në nervin e dëgjimit) është deri tani alternativa më efektive për trajtimin e HL të rëndë, ndërsa një aparat dëgjimi (një pajisje elektronike e jashtme që konverton dhe amplifikon valët e zërit) mund të ndihmojë pacientët me HL të moderuar.Megjithatë, aktualisht nuk ka ilaçe të disponueshme për të trajtuar HL trashëgimore (GHL).Vitet e fundit, terapia gjenetike ka marrë vëmendje në rritje si një qasje premtuese për trajtimin e mosfunksionimit të veshit të brendshëm.
Fig1.Shpërndarja e llojit të variacionit të lidhur me shurdhim.[1]
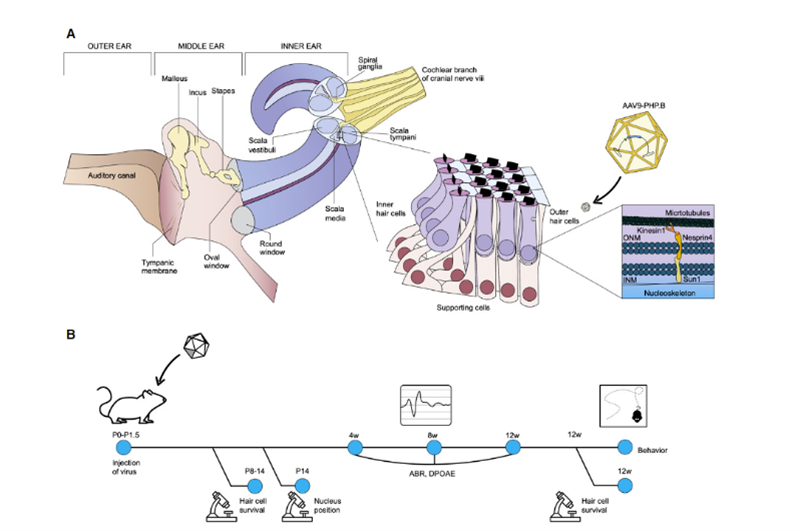
Kohët e fundit, shkencëtarët nga Instituti Salk dhe Universiteti i Sheffield publikuan një rezultat kërkimor në Terapia Molekulare – Metodat dhe Zhvillimi Klinik [2], i cili tregoi perspektiva të gjera aplikimi për terapinë gjenetike in vivo të shurdhimit të trashëguar.Uri Manor, asistent profesor kërkimor në Institutin Salk dhe drejtor i Qendrës Waitt për Biofotonikën e Avancuar, tha se ai kishte lindur me humbje të rëndë të dëgjimit dhe mendonte se rivendosja e dëgjimit do të ishte një dhuratë e mrekullueshme.Hulumtimi i tij i mëparshëm zbuloi se Eps8 është një proteinë rregulluese e aktinës me aktivitete lidhëse dhe mbuluese të aktinës;në qelizat e flokëve koklear, kompleksi proteinik i formuar nga Eps8 me MYO15A, WHIRLIN, GPSM2 dhe GNAI3 ekziston kryesisht.Prandaj, Eps8 mund të rregullojë gjatësinë e stereocilisë së qelizave të flokëve, e cila është thelbësore për funksionin normal të dëgjimit;Fshirja ose mutacioni i Eps8 do të çojë në stereocilia të shkurtra, të cilat e bëjnë atë të paaftë të konvertojë siç duhet tingullin në sinjale elektrike për perceptimin e trurit, gjë që nga ana tjetër çon në shurdhim..Në të njëjtën kohë, bashkëpunëtori Walter Marcotti, një profesor në Universitetin e Sheffield, zbuloi se qelizat e flokëve nuk mund të zhvillohen normalisht në mungesë të Eps8.Në këtë studim, Manor dhe Marcotti u bashkuan për të hetuar nëse shtimi i Eps8 në qelizat stereociliare mund të rivendoste funksionin e tyre dhe, nga ana tjetër, të përmirësonte dëgjimin tek minjtë.Ekipi hulumtues përdori vektorin e virusit të lidhur me adeno (AAV) Anc80L65 për të dhënë sekuencën koduese që përmban EPS8 të tipit të egër në kokleën e minjve P1-P2 të porsalindur Eps8-/- me anë të injektimit të membranës së dritares së rrumbullakët;në qelizat e qimeve koklear të miut Funksioni i stereociliave u riparua para se të maturoheshin;dhe efekti i riparimit u karakterizua nga teknologjia e imazhit dhe matja e stereocilisë.Rezultatet treguan se Eps8 rriti gjatësinë e stereocilisë dhe rivendosi funksionin e qelizave të flokëve në qelizat me frekuencë të ulët.Ata zbuluan gjithashtu se, me kalimin e kohës, qelizat dukej se humbën aftësinë e tyre për t'u shpëtuar nga kjo terapi gjenetike.Implikimi është se ky trajtim mund të ketë nevojë të administrohet në mitër, pasi qelizat e flokëve Eps8-/- mund të kenë maturuar ose grumbulluar dëmtime përtej riparimit pas lindjes së minjve."Eps8 është një proteinë me shumë funksione të ndryshme dhe ka ende shumë për të eksploruar," tha Manor.Hulumtimet e ardhshme do të përfshijnë hetimin e efektit të terapisë gjenetike Eps8 në rivendosjen e dëgjimit në faza të ndryshme zhvillimi dhe nëse mund të jetë e mundur të zgjaten mundësitë e trajtimit.Rastësisht, në nëntor 2020, profesori KarenB Avraham i Universitetit të Tel Avivit në Izrael publikoi rezultatet e tij në revistën EMBO Molecular Medicine [3], duke përdorur një teknologji novatore të terapisë gjenetike për të krijuar një virus sintetik të padëmshëm të lidhur me adeno AAV9-PHP.B, Defekti i gjenit në qelizat e flokëve të minjve Syne4-/- u riparua duke injektuar një virus që mbart sekuencën koduese të Syne4 në veshin e brendshëm të minjve, duke e lejuar atë të hyjë në qelizat e flokëve dhe të lëshojë materialin gjenetik të bartur, duke i lejuar ata të maturohen dhe të funksionojnë normalisht (si në Fig. 2).
Fig2.Paraqitja skematike e anatomisë së veshit të brendshëm, me fokus në organin e Corti dhe funksionin qelizor të nesprin-4.
Mund të shihet se përdorimi i terapisë gjenetike për të arritur qëllimin e trajtimit të sëmundjeve trashëgimore në nivel gjenesh duke futur, hequr ose korrigjuar ndonjë gjen të mutuar për trajtim (domethënë kontrolli i ndryshimeve gjenetike në sëmundje) ka një efekt të lartë klinik.perspektivat e aplikimit.Metodat aktuale të terapisë gjenetike për shurdhim me mangësi gjenetike mund të ndahen në kategoritë e mëposhtme:
zëvendësimi i gjenit
Zëvendësimi i gjeneve është padyshim forma më "e drejtpërdrejtë" e terapisë gjenetike, e bazuar në identifikimin dhe zëvendësimin e një gjeni të dëmtuar me një kopje normale ose të llojit të egër të gjenit.Studimi i parë i suksesshëm i terapisë gjenetike të veshit të brendshëm për humbjen e dëgjimit të shkaktuar nga fshirja e gjenit të transportuesit vezikular të glutamatit 3 (VGLUT3);Shpërndarja e ndërmjetësuar nga AAV1 e mbishprehjes ekzogjene të VGLUT3 në qelizat e qimeve të veshit të brendshëm (IHCs) mund të rezultojë në rikuperim të qëndrueshëm të dëgjimit, rikuperim të pjesshëm të morfologjisë sinaptike të shiritit dhe përgjigje konvulsive [4].Megjithatë, në shembujt që përfshijnë dy zëvendësimet e gjeneve të dorëzuara nga AAV të përshkruara në hyrjen e mësipërme, është e rëndësishme të theksohet se modelet e miut të përdorura për lloje të caktuara të çrregullimeve të humbjes së dëgjimit të trashëguar të fshirjes së gjeneve janë përkohësisht të ndryshme nga njerëzit, dhe te minjtë P1, veshi i brendshëm është në fazën e pjekur të zhvillimit.Në të kundërt, njerëzit lindin me një vesh të brendshëm të pjekur.Ky ndryshim parandalon aplikimin e mundshëm të rezultateve të miut në trajtimin e çrregullimeve të shurdhim të trashëguar të njeriut, përveç nëse terapia gjenetike i jepet veshëve të pjekur të miut.
Redaktimi i gjeneve: CRISPR/Cas9
Krahasuar me "zëvendësimin e gjeneve", zhvillimi i teknologjisë së redaktimit të gjeneve ka sjellë agimin e trajtimit të sëmundjeve gjenetike nga rrënja.E rëndësishmja, metoda e redaktimit të gjeneve plotëson mangësitë e metodave tradicionale të terapisë gjenetike të mbishprehjes, të cilat nuk janë të përshtatshme për sëmundjet dominuese të trashëguara të shurdhimit, dhe problemin që metoda e mbishprehjes nuk zgjat shumë.Pasi studiuesit kinezë eliminuan në mënyrë specifike alelin mutant Myo6C442Y në minjtë Myo6WT/C442Y duke përdorur sistemin e modifikimit të gjeneve AAV-SaCas9-KKH-Myo6-g2, dhe brenda 5 muajve nga nokauti, minjtë funksioni dëgjimor i modelit u rivendos;Në të njëjtën kohë, u vu re gjithashtu se shkalla e mbijetesës së qelizave të flokëve në veshin e brendshëm u përmirësua, forma e qerpikëve u bë e rregullt dhe treguesit elektrofiziologjikë u korrigjuan [5].Ky është studimi i parë në botë që përdor teknologjinë CRISPR/Cas9 për trajtimin e shurdhimit të trashëguar të shkaktuar nga mutacioni i gjenit Myo6, dhe është një progres i rëndësishëm kërkimor i teknologjisë së redaktimit të gjeneve për trajtimin e shurdhësisë trashëgimore.Përkthimi klinik i trajtimit ofron një bazë solide shkencore.
Metodat e dhënies së terapisë gjenetike
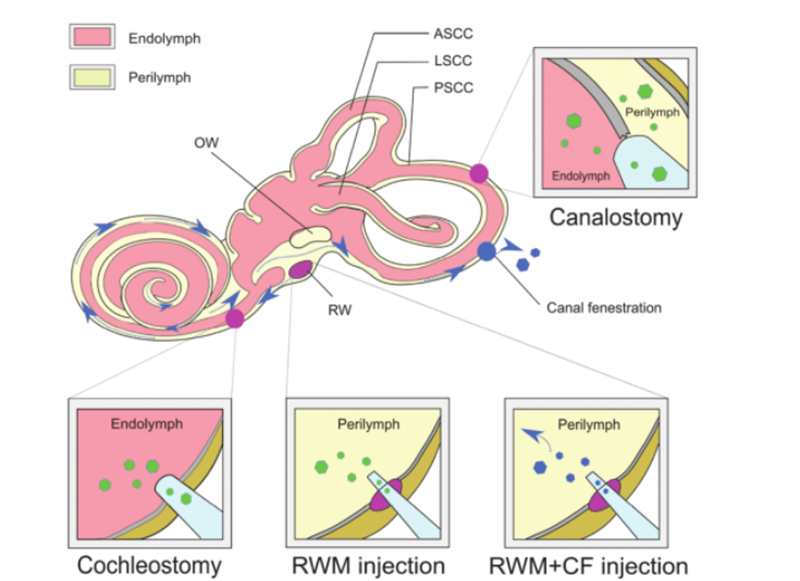
Në mënyrë që terapia gjenetike të jetë e suksesshme, molekulat e ADN-së të zhveshur nuk mund të depërtojnë në qeliza në mënyrë efektive për shkak të hidrofilitetit të tyre dhe ngarkesës negative të grupeve të fosfatit, dhe për të siguruar integritetin e molekulave të acidit nukleik të plotësuar, duhet zgjedhur një metodë e sigurt dhe efektive.ADN-ja e plotësuar shpërndahet në qelizën ose indin e synuar.AAV përdoret gjerësisht si mjet shpërndarjeje për trajtimin e sëmundjeve për shkak të efektit të tij të lartë infektiv, imunogjenitetit të ulët dhe tropizmit të gjerë ndaj llojeve të ndryshme të indeve.Aktualisht, një pjesë e madhe e punës kërkimore ka përcaktuar tropizmin e nëntipave të ndryshëm të AAV në lidhje me llojet e ndryshme të qelizave në kokleën e miut.Përdorimi i karakteristikave të shpërndarjes AAV të kombinuara me promovues specifikë të qelizave mund të arrijë shprehje specifike të qelizës, e cila mund të zvogëlojë efektet jashtë objektivit.Përveç kësaj, si një alternativë ndaj vektorëve tradicionalë AAV, vektorët e rinj sintetikë AAV janë duke u zhvilluar vazhdimisht dhe tregojnë aftësi superiore transduksioni në veshin e brendshëm, nga të cilët AAV2/Anc80L65 është më i përdoruri.Metodat e shpërndarjes jovirale mund të ndahen më tej në metoda fizike (mikroinjektim dhe elektroporim) dhe metoda kimike (me bazë lipide, me bazë polimere dhe nanogrimca ari).Të dyja qasjet janë përdorur në trajtimin e çrregullimeve trashëgimore të shurdhimit dhe kanë treguar avantazhe dhe kufizime të ndryshme.Përveç mjetit të shpërndarjes për terapinë gjenetike si mjet, mund të përdoren qasje të ndryshme për administrimin e gjenit in vivo bazuar në lloje të ndryshme të qelizave të synuara, rrugëve të administrimit dhe efikasitetit terapeutik.Struktura e ndërlikuar e veshit të brendshëm e bën të vështirë arritjen e qelizave të synuara dhe shpërndarja e agjentëve të modifikimit të gjenomit është e ngadaltë.Labirinti membranor ndodhet brenda labirintit kockor të kockës së përkohshme dhe përfshin kanalin koklear, kanalin gjysmërrethor, utrikulin dhe balonën.Izolimi i tij relativ, qarkullimi minimal limfatik dhe ndarja nga gjaku nga një pengesë e labirintit të gjakut kufizojnë shpërndarjen sistematike efektive të terapisë vetëm tek minjtë neonatalë.Për të marrë titrat viralë të përshtatshëm për terapi gjenetike, është i nevojshëm injektimi i drejtpërdrejtë lokal i vektorëve viralë në veshin e brendshëm.Rrugët e vendosura të injektimit përfshijnë [6]: (1) membrana e dritares së rrumbullakët (RWM), (2) trakeostomia, (3) kokleostomia endolimfatike ose perilimfatike, (4) membrana e dritares së rrumbullakët plus mbështjellja e tubit (CF) (si në Fig. 3).
Fig3.Shpërndarja e veshit të brendshëm të terapisë gjenetike.
Megjithëse janë bërë shumë përparime në terapinë gjenetike, bazuar në qëllimet klinike të përkthimit, duhet bërë më shumë punë përpara se terapia gjenetike të bëhet një opsion trajtimi i linjës së parë për pacientët me sëmundje gjenetike, veçanërisht në zhvillimin e vektorëve të sigurt dhe efektiv dhe metodës së shpërndarjes.Por ne besojmë se në të ardhmen e afërt, këto lloj trajtimesh do të bëhen një element kryesor i terapisë së personalizuar dhe do të kenë një ndikim jashtëzakonisht pozitiv në jetën e njerëzve me çrregullime gjenetike dhe familjeve të tyre.
Foregene ka lançuar gjithashtu një komplet shqyrtimi me performancë të lartë për gjenet e synuara, i cili është i shpejtë dhe mund të kryejë reaksione të transkriptimit të kundërt dhe qPCR pa nxjerrjen e ARN-së.
Lidhjet e produktit
Kompleti Cell Direct RT-qPCR — Taqman/SYBR GREEN I
Për më shumë informacion mbi produktin, ju lutemi kontaktoni:
Koha e postimit: Shtator-02-2022