1. Njohuritë bazë (nëse dëshironi të shihni pjesën eksperimentale, ju lutemi kaloni drejtpërdrejt në pjesën e dytë)
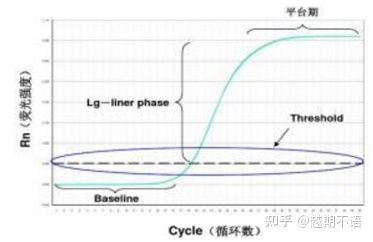
Si një reaksion derivat i PCR-së konvencionale, PCR në kohë reale kryesisht monitoron ndryshimin e sasisë së produktit të amplifikimit në çdo cikël të reaksionit të amplifikimit PCR në kohë reale përmes ndryshimit të sinjalit të fluoreshencës dhe analizon në mënyrë sasiore shabllonin fillestar përmes marrëdhënies midis vlerës ct dhe kurbës standarde.
Të dhënat specifike të RT-PCR janëbazë, pragu i fluoreshencësdheVlera Ct.
| bazë: | Vlera e fluoreshencës e ciklit 3-15 është vija bazë (bazë), e cila shkaktohet nga gabimi i herëpashershëm i matjes. |
| Pragu (pragu): | I referohet kufirit të zbulimit të fluoreshencës të vendosur në një pozicion të përshtatshëm në rajonin e rritjes eksponenciale të kurbës së amplifikimit, përgjithësisht 10 herë më shumë se devijimi standard i vijës bazë. |
| Vlera e CT: | Është numri i cikleve PCR kur vlera e fluoreshencës në çdo tub reaksioni arrin pragun. Vlera Ct është në përpjesëtim të zhdrejtë me sasinë e shabllonit fillestar. |
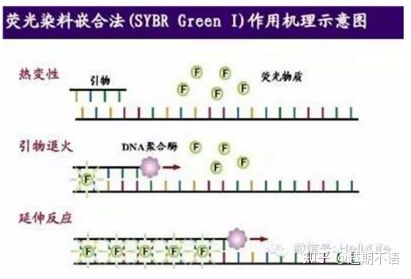
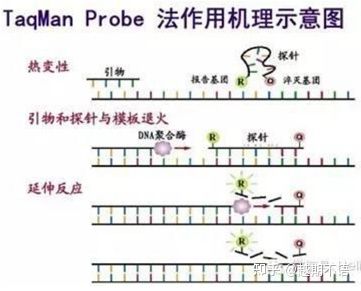
Metodat e zakonshme të etiketimit për RT-PCR:
| metodë | avantazh | mangësi | fushëveprimi i aplikimit |
| SYBR GjelbërⅠ | Zbatueshmëri e gjerë, e ndjeshme, e lirë dhe e përshtatshme | Kërkesat për abetare janë të larta, të prirura ndaj brezave jo specifikë | Është i përshtatshëm për analiza sasiore të gjeneve të ndryshme të synuara, kërkime mbi shprehjen e gjeneve dhe kërkime mbi kafshët dhe bimët rekombinante transgjenike. |
| TaqMan | Specifikimi i mirë dhe përsëritshmëri e lartë | Çmimi është i lartë dhe i përshtatshëm vetëm për qëllime specifike. | Zbulimi i patogjenit, hulumtimi i gjeneve të rezistencës ndaj ilaçeve, vlerësimi i efikasitetit të barnave, diagnoza e sëmundjeve gjenetike. |
| fener molekular | Specifikimi i lartë, fluoreshencë, sfond i ulët | Çmimi është i lartë, është i përshtatshëm vetëm për një qëllim specifik, dizajni është i vështirë dhe çmimi është i lartë. | Analiza e gjeneve specifike, analiza SNP |
2. Hapat eksperimentale
2.1 Rreth grupimit eksperimental- duhet të ketë puse të shumta në grup dhe duhet të ketë përsëritje biologjike.
| ① | Kontrolli bosh | Përdoret për të zbuluar statusin e rritjes së qelizave në eksperimente |
| ② | SiRNA e kontrollit negativ (sekuenca jo specifike e siRNA) | Demonstroni specifikën e veprimit të ARNi.siRNA mund të nxisë përgjigje jo specifike ndaj stresit në një përqendrim prej 200nM. |
| ③ | Kontrolli i reagentit të transfektimit | Përjashtoni toksicitetin e reagjentit të transfektimit në qeliza ose efektin në shprehjen e gjenit të synuar |
| ④ | siRNA kundër gjenit të synuar | Rrëzoni shprehjen e gjenit të synuar |
| ⑤ (opsionale) | siRNA pozitive | Përdoret për të zgjidhur problemet e sistemit eksperimental dhe operacional |
| ⑥ (opsionale) | SiRNA kontrolluese fluoreshente | Efikasiteti i transfektimit të qelizave mund të vërehet me mikroskop |
2.2 Parimet e projektimit të abetares
| Madhësia e fragmentit të përforcuar | Preferohet në 100-150 bp |
| Gjatësia e Abetares | 18-25 bp |
| Përmbajtja GC | 30%-70%, mundësisht 45%-55% |
| Vlera Tm | 58-60 ℃ |
| Sekuenca | Shmangni T/C të vazhdueshme;A/G e vazhdueshme |
| 3 sekuenca fundore | Shmangni GC rich ose AT rich;baza e terminalit preferohet të jetë G ose C;është më mirë të shmangni T |
| Komplementariteti | Shmangni sekuencat plotësuese të më shumë se 3 bazave brenda primerit ose midis dy abetareve |
| Specifikimi | Përdorni kërkimin e shpërthimit për të konfirmuar specifikën e primerit |
①SiRNA është specifike për speciet dhe sekuencat e specieve të ndryshme do të jenë të ndryshme.
②SiRNA është i paketuar në pluhur të tharë në ngrirje, i cili mund të ruhet në mënyrë të qëndrueshme për 2-4 javë në temperaturën e dhomës.
2.3 Mjetet ose reagentët që duhet të përgatiten paraprakisht
| Primer (referencë e brendshme) | Duke përfshirë dy përpara dhe mbrapa |
| Primerë (gjeni i synuar) | Duke përfshirë dy përpara dhe mbrapa |
| ARN e synuar Si (3 shirita) | Në përgjithësi, kompania do të sintetizojë 3 shirita dhe më pas do të zgjedhë një nga tre me anë të RT-PCR |
| Kompleti i transfeksionit | Lipo2000 etj. |
| Kompleti i nxjerrjes së shpejtë të ARN-së | Për nxjerrjen e ARN-së pas transfektimit |
| Kompleti i shpejtë i transkriptimit të kundërt | për sintezën e cADN-së |
| Kompleti i përforcimit PCR | 2×Super SYBR jeshile Përzierje Master qPCR |
2.4 Lidhur me çështjet që duhet t'u kushtohet vëmendje në hapat specifikë eksperimentalë:
① procesi i transfektimit të siRNA
1. Për shtrimin, mund të zgjidhni pllakë 24 pusesh, pllakë 12 pusesh ose pllakë 6 pusesh (përqendrimi mesatar i ARN-së i propozuar në çdo pus të një pllake 24 pusesh është rreth 100-300 ng/uL), dhe dendësia optimale e transfektimit të qelizave është deri në 60%-80% ose më shumë
2. Hapat e transfektimit dhe kërkesat specifike janë rreptësisht në përputhje me udhëzimet.
3. Pas transfektimit, mostrat mund të mblidhen brenda 24-72 orëve për zbulimin e mRNA (RT-PCR) ose zbulimin e proteinave brenda 48-96 orëve (WB)
② procesi i nxjerrjes së ARN-së
1. Parandalimi i kontaminimit nga enzimat ekzogjene.Kryesisht përfshin mbajtjen e maskave dhe dorezave në mënyrë rigoroze;duke përdorur majat e pipetave të sterilizuara dhe tubat EP;uji i përdorur në eksperiment duhet të jetë pa RNase.
2. Rekomandohet të bëni dy herë siç sugjerohet në kompletin e nxjerrjes së shpejtë, gjë që do të përmirësojë vërtet pastërtinë dhe rendimentin.
3. Lëngu i mbeturinave nuk duhet të prekë kolonën e ARN-së.
③ Kuantifikimi i ARN-së
Pasi të nxirret ARN, ajo mund të matet drejtpërdrejt me Nanodrop dhe leximi minimal mund të jetë deri në 10ng/ul.
④ Procesi i kundërt i transkriptimit
1. Për shkak të ndjeshmërisë së lartë të RT-qPCR, duhet të bëhen të paktën 3 puse paralele për çdo mostër për të parandaluar që Ct pasues të jetë shumë i ndryshëm ose SD të jetë shumë i madh për analiza statistikore.
2. Mos e ngrini dhe shkrini përzierjen Master në mënyrë të përsëritur.
3. Çdo tub/vrimë duhet të zëvendësohet me një majë të re!Mos përdorni vazhdimisht të njëjtën majë të pipetës për të shtuar mostra!
4. Filmi i ngjitur në pllakën me 96 pusi pas shtimit të kampionit duhet të lëmohet me një pjatë.Është mirë që të centrifugohet përpara se ta vendosni në makinë, në mënyrë që lëngu në murin e tubit të rrjedhë poshtë dhe të largojë flluskat e ajrit.
⑤Analiza e zakonshme e kurbës
| Nuk ka periudhë të rritjes logaritmike | Ndoshta përqendrim i lartë i shabllonit |
| Nuk ka vlerë CT | Hapat e gabuar për zbulimin e sinjaleve fluoreshente; degradimi i primerëve ose sondave - integriteti i tij mund të zbulohet me elektroforezë PAGE; sasi e pamjaftueshme e shabllonit; degradimi i shablloneve – shmangia e futjes së papastërtive dhe ngrirja dhe shkrirja e përsëritur në përgatitjen e mostrës; |
| Ct>38 | Efikasitet i ulët i amplifikimit;Produkti PCR është shumë i gjatë;komponentë të ndryshëm të reaksionit degradohen |
| Lakorja e amplifikimit linear | Sondat mund të degradohen pjesërisht nga cikle të përsëritura ngrirje-shkrirje ose ekspozimi i zgjatur ndaj dritës |
| Dallimi në vrimat e dyfishta është veçanërisht i madh | Tretësira e reaksionit nuk është shkrirë plotësisht ose tretësira e reaksionit nuk është e përzier;banja termale e instrumentit PCR është e ndotur nga substanca fluoreshente |
2.5 Rreth analizës së të dhënave
Analiza e të dhënave të qPCR mund të ndahet në kuantifikimin relativ dhe atë absolut.Për shembull, qelizat në grupin e trajtimit krahasuar me qelizat në grupin e kontrollit,
Sa herë ndryshon mARN e gjenit X, ky është kuantifikimi relativ;në një numër të caktuar qelizash, mARN e gjenit X
Sa kopje ka, ky është sasia absolute.Zakonisht ajo që ne përdorim më shumë në laborator është metoda relative sasiore.Zakonisht,metoda 2-ΔΔctpërdoret më së shumti në eksperimente, kështu që vetëm kjo metodë do të prezantohet në detaje këtu.
Metoda 2-ΔΔct: Rezultati i marrë është ndryshimi në shprehjen e gjenit të synuar në grupin eksperimental në raport me gjenin e synuar në grupin e kontrollit.Kërkohet që efikasiteti i amplifikimit të gjenit të synuar dhe gjenit të brendshëm të referencës të jetë afër 100%, dhe devijimi relativ nuk duhet të kalojë 5%.
Metoda e llogaritjes është si më poshtë:
Grupi i kontrollit Δct = vlera ct e gjenit të synuar në grupin e kontrollit – vlera ct e gjenit të brendshëm të referencës në grupin e kontrollit
Δct grupi eksperimental = vlera ct e gjenit të synuar në grupin eksperimental – vlera ct e gjenit të brendshëm të referencës në grupin eksperimental
ΔΔct=Δct grup eksperimental-Grup kontrolli Δct
Së fundi, llogaritni shumëfishin e ndryshimit në nivelin e shprehjes:
Ndrysho Fold=2-ΔΔct (që korrespondon me funksionin excel është POWER)
Produkte të ngjashme:
Koha e postimit: Maj-20-2023