Vaksina mRNA e Pfizer për COVID ka rindezur pasionin për përdorimin e acidit ribonukleik (ARN) si një objektiv terapeutik.Megjithatë, synimi i ARN-së me molekula të vogla është jashtëzakonisht sfidues.
ARN ka vetëm katër blloqe ndërtimi: adeninë (A), citozinë (C), guaninë (G) dhe uracil (U) që zëvendëson timinën (T) që gjendet në ADN.Kjo e bën selektivitetin e barnave një pengesë pothuajse të pakapërcyeshme.Në të kundërt, ekzistojnë 22 aminoacide natyrale që përbëjnë proteinat, gjë që shpjegon pse shumica e barnave që synojnë proteinat kanë selektivitet relativisht të mirë.
Struktura dhe funksioni i ARN
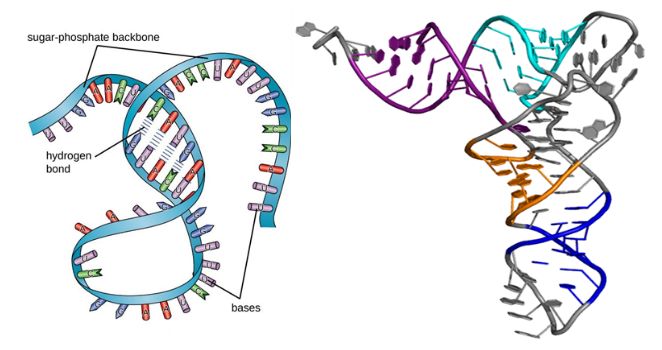
Ashtu si proteinat, molekulat e ARN-së kanë struktura dytësore dhe terciare, siç tregohet në figurën më poshtë.Edhe pse ato janë makromolekula me një zinxhir, struktura e tyre dytësore merr formë kur çiftimi i bazës shkakton fryrje, sythe dhe spirale.Më pas, palosja tredimensionale çon në strukturën terciare të ARN-së, e cila është thelbësore për stabilitetin dhe funksionin e saj.
Figura 1. Struktura e ARN
Ekzistojnë tre lloje të ARN-së:
- ARN e dërguar (mRNA)transkripton informacionin gjenetik nga ADN-ja dhe transferohet si një sekuencë bazë në ribozom;l
- ARN ribozomale (rARN)është pjesë e organeleve sintetizuese të proteinave të quajtura ribozome, të cilat eksportohen në citoplazmë dhe ndihmojnë në përkthimin e informacionit në mARN në proteina;
- ARN transferuese (tRNA)është lidhja midis mARN-së dhe zinxhirit aminoacid që përbën proteinën.
Targetimi i ARN-së si një objektiv terapeutik është shumë tërheqës.Është zbuluar se vetëm 1.5% e gjenomit tonë përkthehet përfundimisht në proteina, ndërsa 70%-90% transkriptohet në ARN.Molekulat e ARN-së janë më të rëndësishmet për të gjithë organizmat e gjallë.Sipas "dogmës qendrore" të Francis Crick, roli më kritik i ARN-së është të përkthejë informacionin gjenetik nga ADN-ja në proteina.Përveç kësaj, molekulat e ARN-së kanë edhe funksione të tjera, duke përfshirë:
- Duke vepruar si molekula përshtatëse në sintezën e proteinave;l
- Shërben si një lajmëtar midis ADN-së dhe ribozomit;l
- Ata janë bartës të informacionit gjenetik në të gjitha qelizat e gjalla;l
- Promovimi i përzgjedhjes ribozomale të aminoacideve të duhura, e cila është e nevojshme për sintetizimin e proteinave të rejain vivo.
Antibiotikët
Pavarësisht se u zbulua që në vitet 1940, mekanizmi i veprimit të shumë antibiotikëve nuk u sqarua deri në fund të viteve 1980.Është zbuluar se një pjesë e madhe e antibiotikëve veprojnë duke u lidhur me ribozomet bakteriale për t'i parandaluar ata të prodhojnë proteinat e duhura, duke vrarë kështu bakteret.
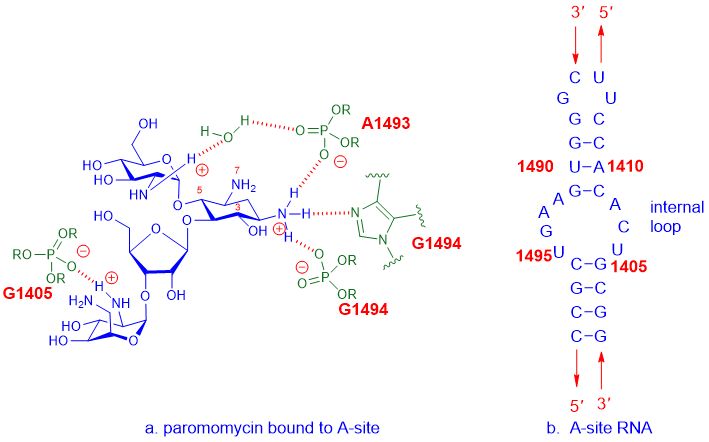
Për shembull, antibiotikët aminoglikozidë lidhen me zonën A të 16S rRNA, e cila është pjesë e nën-njësisë së ribozomit 30S, dhe më pas ndërhyjnë në sintezën e proteinave për të ndërhyrë në rritjen e baktereve, duke çuar përfundimisht në vdekjen e qelizave.Vendi A i referohet vendit të aminoacilit, i njohur gjithashtu si vendi pranues i tRNA.Ndërveprimi i detajuar ndërmjet barnave aminoglikozide, si p.shparomomycin, dhe A-site iE. coliARN është paraqitur më poshtë.
Figura 2. Ndërveprimi ndërmjet paromomycinës dhe A-vendit tëE. coliARN
Fatkeqësisht, shumë frenues të faqes A, duke përfshirë barnat aminoglikozide, kanë probleme sigurie si nefrotoksiciteti, ototoksiciteti i varur nga doza dhe ototoksiciteti specifik i pakthyeshëm.Këto toksicitete janë rezultat i mungesës së selektivitetit në barnat aminoglikozide për njohjen e molekulave të vogla të ARN-së.
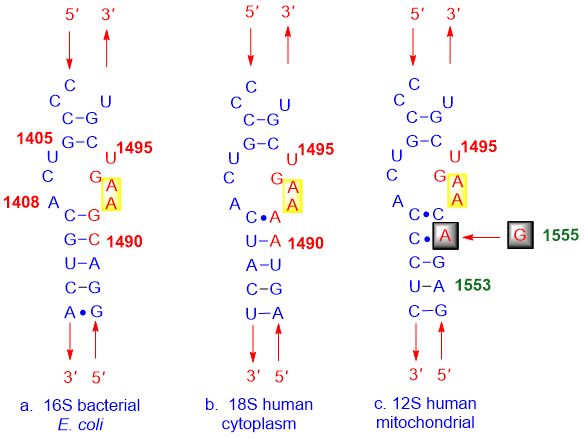
Siç tregohet në figurën më poshtë: (a) struktura e baktereve, (b) membrana qelizore e njeriut dhe (c) vendi A mitokondrial i njeriut janë shumë të ngjashëm, duke i bërë frenuesit e faqes A të lidhen me të gjitha ato.
Figura 3. Lidhja jo selektive e inhibitorit të A-sit
Antibiotikët tetraciklin gjithashtu frenojnë vendndodhjen A të rRNA.Ato pengojnë në mënyrë selektive sintezën e proteinave bakteriale duke u lidhur në mënyrë të kthyeshme në një rajon spirale (H34) në nën-njësinë 30S të kompleksuar me Mg2+.
Nga ana tjetër, antibiotikët makrolidë lidhen pranë vendit të daljes (E-site) të tunelit të ribozomit bakterial për peptidet e sapolindura (NPET) dhe e bllokojnë pjesërisht atë, duke penguar kështu sintezën e proteinave bakteriale.Së fundi, antibiotikët oksazolidinone si p.shlinzolidi(Zyvox) lidhet me një çarje të thellë në nën-njësinë ribozomale bakteriale 50S, e cila është e rrethuar nga nukleotide 23S rRNA.
Oligonukleotide antisense (ASO)
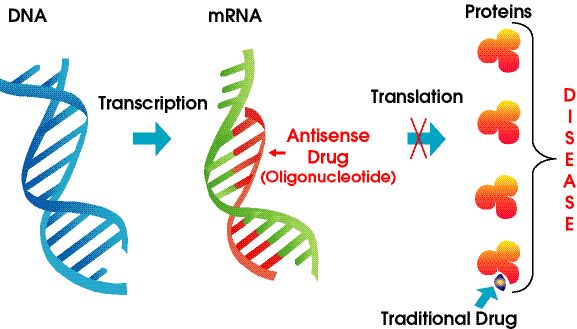
Ilaçet antisense janë polimere të acidit nukleik të modifikuar kimikisht që synojnë ARN-në.Ata mbështeten në çiftimin e bazës Watson-Crick për t'u lidhur me mARN-në e synuar, duke rezultuar në heshtjen e gjeneve, bllokadë sterike ose ndryshim të bashkimit.ASO-të mund të ndërveprojnë me para-ARN-të në bërthamën e qelizës dhe mARN-të e maturuara në citoplazmë.Ata mund të synojnë ekzone, introne dhe rajone të papërkthyera (UTR).Deri më sot, më shumë se një duzinë barnash ASO janë miratuar nga FDA.
Figura 4. Teknologjia Antisense
Barna me molekula të vogla që synojnë ARN-në
Në vitin 2015, Novartis raportoi se ata kishin zbuluar një rregullator bashkimi SMN2 të quajtur Branaplam, i cili rrit lidhjen e U1-pre-mRNA dhe shpëton minjtë SMA.
Nga ana tjetër, Risdiplam i PTC/Roche (Evrysdi) u miratua nga FDA në 2020 për trajtimin e SMA.Ashtu si Branaplam, Risdiplam gjithashtu funksionon duke rregulluar bashkimin e gjeneve përkatëse SMN2 për të prodhuar proteina funksionale SMN.
Degraduesit e ARN-së
RBM qëndron për proteinën e motivit që lidh ARN-në.Në thelb, sulfonamidi i indolit është një ngjitës molekular.Ai rekruton në mënyrë selektive RBM39 në ligazën e ubiquitinit CRL4-DCAF15 E3, duke promovuar poliubiquitinimin e RBM39 dhe degradimin e proteinave.Zhdukja gjenetike ose degradimi i ndërmjetësuar nga sulfonamidi i RBM39 shkakton anomali të rëndësishme të bashkimit në të gjithë gjenomin, duke çuar përfundimisht në vdekjen e qelizave.
ARN-PROTAC-et janë zhvilluar për të degraduar proteinat që lidhen me ARN-në (RBP).PROTAC përdor një lidhës për të lidhur ligand ligazë E3 me ligand ARN, i cili lidhet me ARN dhe RBPs.Meqenëse RBP përmban domene strukturore që mund të lidhen me sekuenca specifike oligonukleotide, ARN-PROTAC përdor një sekuencë oligonukleotide si një ligand për proteinën e interesit (POI).Rezultati përfundimtar është degradimi i RBP-ve.
Kohët e fundit, profesori Matthew Disney i Institutit Scripps të Oqeanografisë shpiku ARN-nëkimerat që synojnë ribonukleazën (RiboTACs).RiboTAC është një molekulë heterofunksionale që lidh një ligand RNase L dhe një ligand ARN me një lidhës.Ai mund të rekrutojë në mënyrë specifike RNase L endogjene në objektiva specifike të ARN-së dhe më pas të eliminojë me sukses ARN-në duke përdorur mekanizmin e zbërthimit të acidit nukleik qelizor (RNase L).
Ndërsa studiuesit mësojnë më shumë rreth ndërveprimit midis molekulave të vogla dhe objektivave të ARN-së, më shumë ilaçe që përdorin këtë metodë do të shfaqen në të ardhmen.
Koha e postimit: Gusht-02-2023